Dichtheid van water waarbij de verhouding tussen de massa en het volume van het water bij kamertemperatuur 998,2 kg/m is3. De dichtheid van elke stof wordt gedefinieerd als de hoeveelheid massa die aanwezig is in het eenheidsvolume van de gegeven stof.
Voor zuiver water is de dichtheid 1 gram/cm 3 of 1000kg/m 3 . De dichtheid van zuiver water varieert met de temperatuur en bereikt zijn hoogste punt bij een temperatuur van 4 °C, oftewel 1000 kg/m3.
De dichtheid van water is maximaal bij 4 °C.
Wat is de dichtheid van water?
De term dichtheid verwijst naar hoeveel volume (ruimte) een object of substantie in beslag neemt in verhouding tot de hoeveelheid materiaal die het bevat (de massa). Een andere manier om aan dichtheid te denken is de hoeveelheid massa per volume-eenheid. Een object met een hoge dichtheid is solide en compact. De SI-eenheid van dichtheid is kg/m3en g/cm3in het CGS-systeem. Het is een intrinsieke eigenschap van materie.
De dichtheid van water is 1 g/cm3wat geen toeval is. Dichtheid is de verhouding tussen de massa van de materie en het volume dat erdoor wordt ingenomen, gebruikt om de dichtheid te berekenen van 1 g water dat 1 cm in beslag neemt3volume. Bovendien hebben de luchtdruk en de atmosferische temperatuur ook invloed op de dichtheid van water.
converteer char naar int java
Deze verschillen in dichtheid zijn echter relatief klein, waardoor je 1 g/cm kunt blijven gebruiken3voor de waterdichtheid, tenzij u zeer specifieke berekeningen moet uitvoeren of het experiment wordt uitgevoerd in omstandigheden met extreme temperaturen of drukken.
De dichtheid van water voor verschillende metrische systemen wordt echter hieronder gegeven:
| Dichtheid van water | Eenheidssysteem | Dichtheid van water |
| Dichtheid van water in g/cm3 | 1 g/cm3 | |
| Dichtheid van water in g/ml | 1 g/ml | |
| Dichtheid van water in kg/m3 | 1000kg/m3 | |
| Dichtheid van water in lb/ft3 | 62,4 lbs/ft3 |
De stof waarvan de dichtheid kleiner is dan water drijft op het water en de stof waarvan de dichtheid groter is dan water zinkt in het water.
De onderstaande afbeelding toont drie containers. In de eerste container is de dichtheid van de kurk minder dan die van water, zodat deze op het water drijft. In de tweede container is de dichtheid van het hout bijna gelijk aan die van water, zodat deze gedeeltelijk in het water wordt ondergedompeld. en in de derde container is de dichtheid van kurk (aluminium) groter dan die van water, zodat het in het water zinkt.
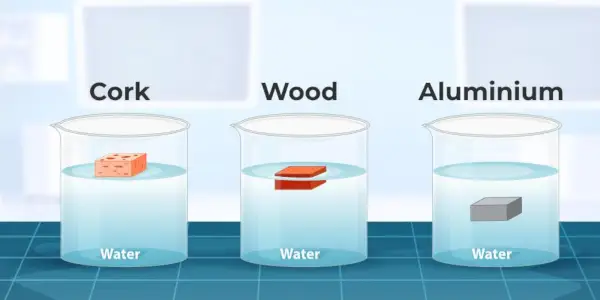
Houd er rekening mee dat deze cijfers voor de waterdichtheid alleen van toepassing zijn op zuiver water. De dichtheid van zout water (zoals de oceanen) varieert afhankelijk van hoeveel zout er in het water is opgelost. De dichtheid van zeewater ligt normaal gesproken tussen 1,02 g/cm33en 1,03 g/cm33, wat iets groter is dan de dichtheid van zuiver water.
Eigenschappen van water
Water is een vreemde vloeistof, het is de belangrijkste vloeistof voor het voortbestaan van de mens. Hieronder worden verschillende eigenschappen van water besproken,
| Dichtheid van water | 997kg/m³ |
|---|---|
| Formule van water | H2O |
| Molaire massa van water | 18,015 g/mol |
| Kookpunt van water | 100 °C |
| Smeltpunt van water | 0 °C |
Dichtheid van waterformule
De dichtheid van water wordt berekend met behulp van de normale dichtheidsformule,
D = M/V
waar,
D is de dichtheid van het water
M is de massa van het water
IN is het volume van het water
We weten dat,
Als het watervolume bij kamertemperatuur 1 ml is, wordt de massa ervan waargenomen als 0,995 gram. Nu is de dichtheid van het water,
D = massa/volume
= 0,995/1
= 0,995 g/ml = 0,995 g/cm33
Leer meer over Dikte En Structuur en eigenschappen van water
Hoe de dichtheid van water berekenen?
Een maatcilinder wordt gebruikt om de dichtheid van water te berekenen. Een lege cilinder wordt genomen en op een machine gewogen. Dit geeft ons de massa van een lege maatcilinder, dat wil zeggen m.
Nu wordt de benodigde hoeveelheid water in de cilinder gedaan en wordt deze opnieuw gewogen. Dit geeft ons de massa van de gevulde maatcilinder, dat wil zeggen m’.
Het verschil tussen de berekende massa's zou ons de massa water opleveren. Dus,
Massa van water (M) = m’ – m
Het watervolume (V) wordt gevonden met behulp van de markering op de cilinder. Het blijkt dat het volume van water bijna gelijk is aan de massa.
Dus als we de formule voor dichtheid gebruiken, krijgen we:
ρ = Massa water/volume water
ρ = M/V [aangezien massa (M) en volume (V) vrijwel gelijk zijn]
ρ = 1 g/ml
Er wordt geconcludeerd dat de dichtheid van water een constante waarde is, dat wil zeggen: 1g/ml of 1 g/cm 3 .
Dichtheid van water bij kamertemperatuur
Bij kamertemperatuur, d.w.z. bij een temperatuur van 20 °C tot 25 °C, is de dichtheid van het water 0,9982 g/cc, of 998,2 kg/m3. De massa van water is bij kamertemperatuur vrijwel gelijk aan het volume en bij kamertemperatuur blijft het water in vloeibare vorm. In zeewater zijn verschillende zouten en mineralen opgelost, waardoor de dichtheid iets hoger is dan die van normaal water. Normaal gesproken is de dichtheid van zeewater ongeveer 1027 kg/m3.
Factoren die de dichtheid van water beïnvloeden
Een aantal factoren kunnen de dichtheid van een stof beïnvloeden. Enkele van de factoren die de waterdichtheid beïnvloeden, worden hieronder opgesomd:
De dichtheid van water is ongeveer 1 gram per kubieke centimeter (1 g/cm).3).
- Hoewel de relatie wordt beschreven als niet-lineair en unimodaal in plaats van monotoon, is deze temperatuurafhankelijk.
- Vloeibaar water heeft de neiging dichter te worden wanneer het wordt afgekoeld vanaf kamertemperatuur, maar toch wordt aangenomen dat zuiver water zijn maximale dichtheid bereikt bij ongeveer 4 °C en dat van 4 °C tot 0 °C de dichtheid van water toeneemt, en dit gedrag wordt het afwijkende gedrag genoemd. gedrag van water.
- Naarmate het meer afkoelt, heeft het de neiging uit te zetten en minder dicht te worden. Water is dus een vreemde vloeistof die bij afkoeling tot een bepaald punt dichter wordt en bij verdere afkoeling begint uit te zetten.
Dichtheid van water op verschillende temperatuurschalen
De volgende grafiek toont de dichtheid van water (in g/cm3) bij verschillende temperaturenwaarden (in °C)
| Temperatuur (in C) | Dichtheid van water (g/cm3) |
|---|---|
| -30° | 0,98385 |
| -20° | 0,99355 |
| -10° | 0,99817 |
| 0° | 0,99987 |
| 4,0° | 1,00000 |
| 10e | 0,99975 |
| 21° | 0,99802 |
| 48,9° | 0,98870 |
| 60° | 0,98338 |
| 71,1° | 0,97729 char om Java te stringen |
| 82,2° | 0,97056 |
| 93,3° | 0,96333 |
| 100° | 0,95865 |
Zoals is waargenomen heeft water een dichtheid die precies gelijk is aan 1 g/cm3alleen bij 4 °C. Er is ook waargenomen dat de dichtheid van water afneemt naarmate de temperatuur stijgt. IJs heeft een lagere dichtheid dan water, waardoor de dichtheid van water afneemt. Dit is de reden waarom ijs op het water drijft en waarom ijsblokjes niet zomaar op de bodem van een glas water vallen als je ze erin doet.
Abnormale uitzetting van water
Water gedraagt zich abnormaal bij verwarming, d.w.z. de uitzetting ervan is niet lineair. De dichtheid ervan nam eerst toe van 0 °C naar 4 °C en begon daarna af te nemen naarmate het volume begon toe te nemen.
Nu is het duidelijk dat de dichtheid maximaal is bij 4 °C
De maximale dichtheid van het water ligt bij 4°C, wat neerkomt op 1 g/cm23of 1000 kg/m3.
Dichtheid versus temperatuur
Omdat de dichtheid verandert met de temperatuur, heeft water geen absolute dichtheid. De vloeibare vorm heeft een grotere dichtheid dan de vaste vorm. Als u wilt weten hoe de dichtheid varieert met de temperatuur, bekijkt u de onderstaande grafiek van dichtheid versus temperatuur.
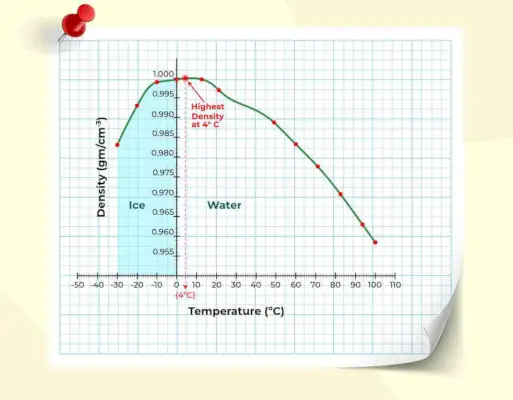
Dichtheid van water Maximaal bij 4 °C?
Water is een vreemde vloeistof en gedraagt zich abnormaal. De dichtheid van water is maximaal bij 4 ° C en dit kan als volgt worden verklaard:
- Terwijl het water bevriest, komen de deeltjes dichterbij totdat ze hun maximale dichtheid bereiken bij 4°C. Bij deze temperatuur is water alleen in vloeibare toestand.
- Nadat de temperatuur hierdoor verder is gedaald, heeft het water de neiging te bevriezen en een vaste toestand te verwerven.
- Je zou kunnen denken dat vast water dichter zou zijn, maar toen het water begon te bevriezen, krijgt het een kooiachtige structuur die uiteindelijk het volume van het water vergroot en dit is de reden waarom ijs op het water drijft.
- Zoals we nu weten, neemt de dichtheid af als het volume toeneemt. De dichtheid van water neemt dus af na 4°C.
Het is dus duidelijk dat de dichtheid van water maximaal is bij 4°C
Rekening: Formule voor waterdruk
Dichtheid van waterexperiment
Om meer te begrijpen over de dichtheid van water, hoe het zich gedraagt en de vergelijking ervan met andere stoffen. Laten we de onderstaande activiteit uitvoeren:
Neem een kleine hoeveelheid van een aantal vloeistoffen die viskeus zijn als water, b.v. Vloeibare zeep, melk, suikersiroop, honing, ethylalcohol en olijfolie in een reageerbuis. Meng ze goed, zodat elk van de stoffen niet duidelijk kan worden waargenomen.
Laat het nu een paar uur staan, zodat de laag van elke substantie op een bepaald niveau bezinkt, zoals hieronder weergegeven:

Nu is waargenomen dat verschillende stoffen een verschillende dichtheid hebben. Dit houdt in dat elke stof anders weegt voor hetzelfde volume. Omdat hun gewicht varieert, hebben zwaardere stoffen de neiging zich op de bodem te nestelen, zoals honing, en hebben suikerstroop en lichtere stoffen zoals olijfolie en ethylalcohol de neiging bovenaan te drijven.
Dichtheid van gewone vloeistoffen
Verschillende vloeistoffen hebben verschillende dichtheden omdat ze verschillende massa's hebben voor een vast vloeistofvolume. De hieronder besproken tabel vertelt ons de dichtheid van verschillende vloeistoffen bij kamertemperatuur.
| Materiaal | Dichtheid (gram/cm3) |
|---|---|
| Lamp olie | 0,8 |
| Water | 1,0 |
| Melk | 1.03 |
| Vloeibare zeep | 1.06 |
| Honing | 1.42 |
| Glycerine | 1.260 |
| Kwik | 13.55 |
Lees verder,
- De wet van Pascal
- Drijfvermogen
- Het principe van Bernoulli
Opgeloste voorbeelden van de dichtheid van water
Voorbeeld 1: Bereken de dichtheid van water als de massa van de lege maatcilinder 10,2 g is en die van de gevulde maatcilinder 20 g.
Oplossing:
We hebben,
m’ = 20
m = 10,2
Bereken de massa van water.
M = m’ – m
M=20 – 10,2
M = 9,8 gram
Dus volume (V) = 9,8 ml
Met behulp van de formule die we krijgen,
ρ = M/V
= 9,8/9,8
= 1g/ml
Voorbeeld 2: Bereken de massa van de gevulde maatcilinder als de massa van het water 5 g is en de massa van de lege cilinder 15 g.
Oplossing:
We hebben,
M = 5
m = 15
Met behulp van de formule die we hebben,
M = m’ – m
m’ = M + m
m’ = 5 + 15
m’ = 20 gram
De vereiste massa van een gevulde maatcilinder is dus 20 gram
Rekening: Verschil tussen dichtheid en soortelijk gewicht
Dichtheid van water – Veelgestelde vragen
Bij welke temperatuur is de dichtheid van water maximaal?
De dichtheid van water is maximaal bij 4°C of bij 39°F.
Wat is de dichtheid van water?
De dichtheid van een stof wordt gedefinieerd als de massa van die stof verdeeld over een volume-eenheid. Het wordt aangegeven met het symbool rho (ρ). De standaard meeteenheid is kilogram per kubieke meter (kg/m3) en de maatformule wordt gegeven door [M1L-3T0].
Waarom is de dichtheid van water groter dan die van ijs?
De dichtheid van water is groter dan de dichtheid van ijs, want als het water ijs vormt, neemt het volume ervan toe omdat het een kooiachtige structuur vormt
Waarom drijft ijs in water?
Bij ongeveer 4° Celsius heeft water de hoogste dichtheid. IJs drijft omdat het een lagere dichtheid heeft dan vloeibaar water. Bij bevriezing neemt de ijsdichtheid met ongeveer 9% af.
Hoe beïnvloedt temperatuur de dichtheid van water?
De dichtheid van water verandert met de temperatuur. Deze neemt toe als het water wordt afgekoeld tot 4°C en neemt af als de temperatuur boven of onder dit punt komt. Bij 100°C bedraagt de dichtheid bijvoorbeeld ongeveer 958,4 kg/m³, en bij -30°C ongeveer 983,854 kg/m³.
Waarom heeft de dichtheid van water een maximum bij 4°C?
Bij ongeveer 4°C bereikt water zijn maximale dichtheid als gevolg van een evenwicht tussen concurrerende moleculaire krachten. Beneden deze temperatuur begint water uit te zetten terwijl het zich voorbereidt om te bevriezen. Daarom drijft ijs op vloeibaar water.
Heeft de aanwezigheid van zouten en mineralen invloed op de waterdichtheid?
Ja, de dichtheid van water kan toenemen door de aanwezigheid van opgeloste zouten, mineralen en andere stoffen. Zeewater heeft bijvoorbeeld een grotere dichtheid dan zoet water, met typische dichtheden van ongeveer 1027 kg/m³ aan het oppervlak vanwege het zoutgehalte.
Wat is de dichtheid van zeewater?
De dichtheid van zeewater, aan de oppervlakte 1027 kg/m3ongeveer.
Wat is de dichtheid van water bij kamertemperatuur?
De dichtheid van water bij kamertemperatuur is 998,2 kg/m3.
